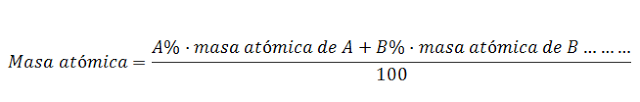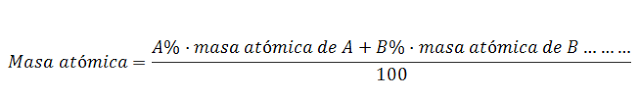Iones , negativos y positivos , aniones y cationes , protones neurtones y electrones, física y química 3º 4º ESO , 1º 2º bachillerato pruebas de acceso y universidad
Isótopos y masa atómica ver explicación
Vimos anteriormente que en un elemento químico todos sus átomos tienen el mismo número atómico .
Isótopos son las formas de un mismo elemento que tienen distinto número másico
Por ejemplo
El 1735Cl 1737Cl son dos isótopos del cloro
Masa atómica Se mide en umas ( unidad de masa atómica) de símbolo u
Gran parte de los elementos químicos presentan isótopos. Por este motivo la masa atómica de un elemento en la tabla periódica indica la masa del átomo promedio de ese elemento, , según la fórmula:
Ejercicios 01 ver solución
El cloro está formado en la naturaleza dos isótopos ,uno con masa atómica 35 u con abundancia del 76%, y el otro con masa atómica 37 u con abundancia isotópica del 24%.¿Cuál es la masa atómica del cloro?
Ejercicios 02 ver solución
El Silicio está formado por un 93% del isótopo de masa atómica 28 u, un 4% del isótopo de masa atómica 29 u, y el resto, por el isótopo de masa atómica 30 u. calcula la masa atómica media del silicio.
Ejercicios 03 ver solución
La plata tiene una masa atómica de 107,87 u. Sabiendo que esta formada por 2 isótopos de masas atómicas 107 y 109 u respectivamente . calcular la abundancia de cada isótopo en la naturaleza