Geometría molecular Tabla , estudiaremos la geometría de las moléculas , Tetraédrica , piramidal trigonal , angular , del agua , Triangular plana , lineal , etc Ejercicios y ejemplos resueltos paso a paso desde cero Química 1 de bachillerato 2 bachillerato y universidad
Esta entrada pertence al TEMA ENLACE QUIMICO EJERCICIOS RESUELTOS
CONTENIDOS PREVIOS NECESARIOS
Estructura de Lewis ejercicios resueltos
GEOMETRÍA MOLECULAR
Pasos a seguir para deducir la geometría molecular mediante la Teoría RPECV , (repulsión de pares de electrones de la capa de valencia )
Paso 1 Realizamos el diagrama de Lewis
Paso 2 Contamos los pares de electrones enlazantes y No enlazantes (libres) del átomo central
Paso 3 Miramos en la tabla
| Teoría de repulsión de pares de electrones de la capa de valencia TRPECV | |||||
| Pares de e– | e– Enlazantes | e– No Enlazantes ( libres) | Estructura | Geometría molecular | Ejemplos |
| 4 | 2 | 2 | Tetraédrica | Angular | H2O,H2S |
| 4 | 3 | 1 | Tetraédrica | Piramidal trigonal | NH3,PCl3 |
| 4 | 4 | 0 | Tetraédrica | Tetraédrica | CH4,SiF4 |
| 3 | 3 | 0 | Triangular plana | Triangular plana | BH3, BF3 |
| 3 | 2 | 1 | Triangular plana | Angular | SO2 |
| 2 | 2 | 0 | Lineal | Lineal | BeH2,CO2 |
| 5 | 5 | 0 | Bipiramidal trigonal | Bipiramidal trigonal | PCl5 |
| 6 | 6 | 0 | Octaédrica | Octaédrica | SF6 |
Si ya eres una máquina ayudanos a crecer compartiéndonos por las redes sociales
Vamos a ver un ejemplo con las geometrías más clásicas
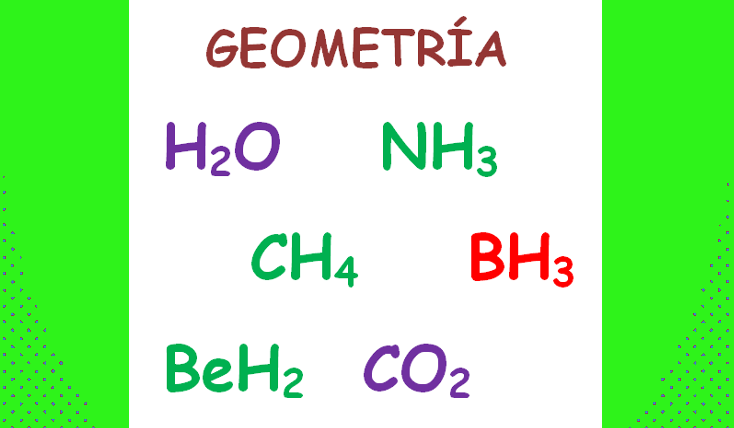
Justifica la geometría de las siguientes moléculas según la teoría RPECV , H2O , NH3 , CH4 , BH3 , BeH2 , CO2
VER SOLUCIÓN
Paso 1 Realizamos el diagrama de Lewis
Paso 2 Contamos los pares de electrones enlazantes y No enlazantes (libres) del átomo central
Paso 3 Miramos en la tabla
| Pares de e– | e– Enlazantes | e– No Enlazantes ( libres) | Estructura | Geometría molecular | Solución |
| 4 | 2 | 2 | Tetraédrica | Angular | |
| 4 | 3 | 1 | Tetraédrica | Piramidal trigonal | |
| 4 | 4 | 0 | Tetraédrica | Tetraédrica | |
| 3 | 3 | 0 | Triangular plana | Triangular plana | |
| 2 | 2 | 0 | Lineal | Lineal |
SIGUE ESTE ENLACE PARA SER UNA MÁQUINA
ENLACE QUIMICO EJERCICIOS RESUELTOS
La geometría también se puede ver por la teoría de
HIBRIDACIÓN
Ejercicios resueltos 01 ver solución
Estudiar la hibridación del Metano CH4 , eteno C2H4 , etino C2H2
Datos C(Z=6) H(Z=1)
Si ya eres una máquina ayudanos a crecer compartiéndonos por las redes sociales
Teoría
Estudiaremos la hibridación del carbono en los casos de que todos los enlaces sean simples , cuando el carbono tenga enlaces doble y cuando tenga enlaces triples
Cuando todos los enlaces del carbono sean simples tendremos una hibridación sp3 , dando lugar a una geometría tetraédrica y todos los solapamientos serán frontales tipo signa
En el caso de que haya un enlace doble , tendremos una hibridación sp2 , ahora como el enlace doble se tiene que producir entre orbitales puros p sin hibridar , ya solo hibridarán 2 orbitales p y un orbital s , luego la hibridación será del tipo sp2 , dando lugar a una geometría plana triangular . El doble enlace estará formado por un solapamiento frontal tipo sigma y por otro solapamiento lateral tipo π
En el caso que haya un enlace triple , tendremos una hibridación sp , ahora como el enlace es triple el carbono tiene que tener dos enlaces p puros sin hibridar sólo se producirá la hibridación entre un orbital p y un orbital s , luego la hibridación será tipo sp , dando lugar a una geometría lineal . El triple enlace estará formado por un solapamiento frontal tipo sigma y dos solapamientos laterales tipo π
OTRAS ENTRADAS QUE TE PUEDEN INTERESAR
Estructura de Lewis Enlace Iónico